Испытания вакцины против COVID прошли триумфально. Теперь нам нужна аналогичная система для антибиотиков
Успех разработки вакцины против COVID-19 и открытие эффективных методов лечения стали возможны только благодаря беспрецедентной координации клинических испытаний. Процесс тестирования, который часто длится более десяти лет, был сокращен до менее чем девяти месяцев. Теперь это должно быть моделью для других серьезных кризисов в области здравоохранения на планете, а именно, устойчивости к противомикробным препаратам (УПП).
Чтобы опережать невирусные микробные угрозы и быстро реагировать на них, пора создать новую перспективную инфраструктуру клинических испытаний. Сеть государственных институтов клинических испытаний могла бы надолго соединить доклиническую академическую изобретательность с лучшими постклиническими коммерческими знаниями и пополнить их новыми антибиотиками. Срочно необходимы действия. Таков вывод исследования, которое провели ученые Ливерпульской школы тропической медицины и Британского центра экологии и гидрологии.
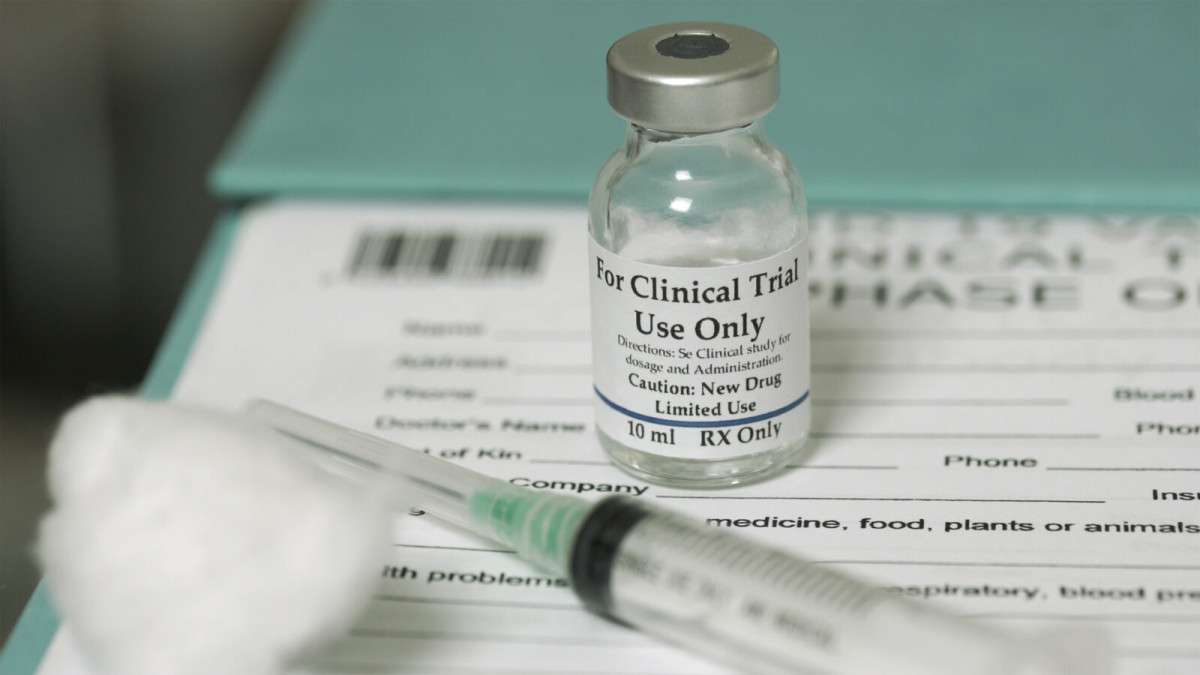 Фото: https://webtopnews.com/
Фото: https://webtopnews.com/
УПП – естественный процесс, при котором бактерии приспосабливаются к сопротивлению антибиотикам, используемым для борьбы с ними. Поэтому он представляет серьезную угрозу для глобального здравоохранения и систем производства продуктов питания. Десятки тысяч людей уже умирают, многие страдают от инфекций, которые когда-то поддались лечению, и проблема быстро растет. Частично ее решение заключается в том, чтобы лучше заботиться об уже имеющихся в нашем распоряжении антибиотиках. Каждый раз, когда используется антибиотик, он создает эволюционное преимущество для бактерий, способных противостоять его воздействию. Со временем это приводит к появлению устойчивой бактериальной популяции. Таким образом, антибиотики – это ограниченный по времени ресурс, который следует использовать с осторожностью.
Привлечение инвесторов
Но существуют хорошо известные экономические препятствия для коммерческих исследований и разработок антибиотиков. Наиболее важным является то, что исследования, испытания и лицензирование новых лекарств обходятся дорого, но новые антибиотики приносят меньше прибыли, чем лекарства от рака или хронических состояний, и их необходимо защищать от чрезмерного использования, чтобы предотвратить резистентность.
Также нет никакой гарантии, что инвестиции в многообещающее соединение, обнаруженное в ходе доклинических исследований, превратится в жизнеспособное лекарство. В настоящее время около 95% многообещающих доклинических соединений, которые проходят испытания на людях, не проходят через так называемую «долину смерти» клинических испытаний до одобрения регулирующих органов. Это связано с тем, что некоторые соединения проявляют незначительный эффект или не проявляют никакого эффекта, другие имеют побочные эффекты, а некоторые разработчики не могут привлечь и удержать объем инвестиций, необходимых для финансирования дорогостоящих клинических испытаний, которые могут занять более 13 лет. Многие другие исследовательские проекты терпят неудачу еще до того, как их протестируют на людях.
Столкнувшись с таким количеством рисков и менее привлекательными перспективами прибыли, чем в случае с другими лекарствами, зачем любому коммерческому разработчику вкладывать средства в исследования антибиотиков? И, чтобы заманить коммерческих инвесторов, Великобритания, США и ЕС вложили более 1,5 миллиарда долларов из государственных средств для субсидирования исследований на ранних этапах и увеличения финансовой отдачи от антибиотиков, которые проходят испытания.
На недавней встрече G7 Великобритания попыталась продвигать так называемую модель подписки на антибиотики, которую она внедрила в 2020 году. Как и в случае с Netflix, правительства больше не будут платить промышленности за использованную таблетку антибиотика (как они это делают сейчас), а только за стоимость этой таблетки обществу. Есть надежда, что гарантированная прибыль и минимальные инвестиционные риски побудят крупные фармацевтические компании реинвестировать в исследования и разработки. Но до сих пор успех традиционных субсидий, ориентированных на рынок, был ограничен, и члены G7 не придерживались прямо британской модели подписки. Хотя они согласились изучить дальнейшее усиление рыночных стимулов.
 Фото: https://rostec.ru/
Фото: https://rostec.ru/
Учимся на COVID-19
В связи с глобальным всплеском устойчивых к противомикробным препаратам организмов, уже охватившим нас, и COVID-19, оказывающим дальнейшее давление на существующие антибиотики в результате сопутствующих и вторичных инфекций, нам срочно требуются новые творческие подходы к поиску лекарств. Одно из решений может состоять в том, чтобы перевернуть существующую модель субсидирования новых антибиотиков с ног на голову. Вместо того, чтобы складывать «все яйца в одну корзину» и финансировать отдельные компании, которые могут или не могут пройти через «долину смерти», эксперты предлагают построить мост через эту долину с сетью государственных институтов. Эти институты смогут проводить клинические испытания и производить ограниченное количество экспериментальных антибиотиков.
Специальная инфраструктура для клинических испытаний антибиотиков сочетает в себе лучшие ноу-хау государственного и частного секторов. Интеллектуальная собственность, полученная в результате государственных исследований, останется в руках общественности, и ученые смогут полностью отдать должное своим открытиям, опубликовав результаты, а не дожидаясь подачи патентных заявок. Помимо защиты соединений от коммерческой неудачи и исчезновения за патентными барьерами, постоянная сеть институтов клинических испытаний также может снизить стоимость и повысить качество испытаний.
На данный момент разработчикам необходимо привлекать крупные суммы венчурного капитала для финансирования коммерческих испытаний. Специализированные институты испытаний антибиотиков снизят риски этого процесса, накопят человеческий опыт в испытании лекарств и значительно снизят затраты на исследования и разработки для государственных и частных разработчиков.
Сделав доступ к общедоступным сетям клинических испытаний зависимым от нацеливания на приоритетные патогены, определенные Всемирной организацией здравоохранения, будут стимулироваться доклинические исследования и разработки, направленные на решение наиболее острых, а не только наиболее прибыльных, проблем здравоохранения. Между тем, клинические испытания могут проводиться в районах с низким доходом, где больше всего нужны новые антибиотики.
По окончании клинического испытания промышленность может быть уполномочена делать то, что у нее получается лучше всего: производить и распространять. Подобно другим государственным услугам, предоставляемым коммерческими компаниями, новые лекарства могут распространяться коммерческими производителями, способными гарантировать экологически безопасное производство и доступные цены на лекарства.
 Фото: https://www.rbc.ru/
Фото: https://www.rbc.ru/
Глобальные ответные меры на вакцину COVID показали важность перспективной общественной инфраструктуры и инвестиций в исследования, чтобы опережать и быстро реагировать на микробные угрозы. Сеть государственных институтов клинических испытаний антибиотиков могла бы сделать это и принести пользу как общественным, так и коммерческим разработчикам. После более чем 30 лет приостановки инноваций и субсидий для остановки-запуска это могло навсегда устранить пробел в испытаниях.
